長生生物官網被黑,黑客:不搞你,對不起祖國的花朵
2018-07-26
2675
原標題:長生生物官網被黑,黑客:不搞你,對不起祖國的花朵
IT之家7月23日消息 根據新浪證券的消息,長生生物官網首頁被黑客攻擊,顯示網站已無法打開,黑客配圖稱“不搞你,對不起祖國的花朵”。
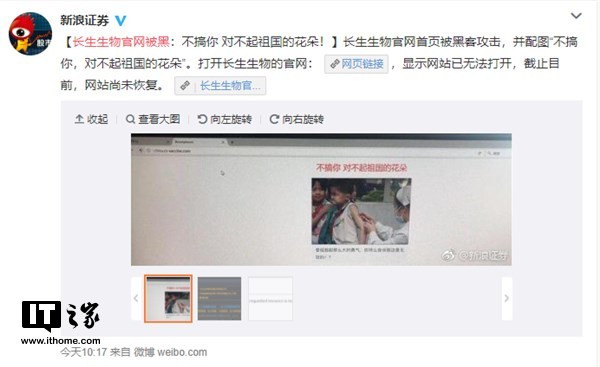
IT之家稍早前曾報道,據國家藥監局網站顯示,7月22日,國家藥監局負責人通報長春長生生物科技有限責任公司違法違規生產凍干人用狂犬病疫苗案件有關情況。
現已查明,企業編造生產記錄和產品檢驗記錄,隨意變更工藝參數和設備。上述行為嚴重違反了《中華人民共和國藥品管理法》《藥品生產質量管理規范》有關規定,國家藥監局已責令企業停止生產,收回藥品GMP證書,召回尚未使用的狂犬病疫苗。國家藥監局會同吉林省局已對企業立案調查,涉嫌犯罪的移送公安機關追究刑事責任。
另外,長生生物也發布了公告,回復深圳證券交易所的關注函。公告中,長生生物稱,對于此次事件的發生感到十分的自責和愧疚,再次向各位接種者和投資者表示深深的歉意。
自媒體“獸樓處”的一篇已消失的文章《疫苗之王》,在周末引爆了人們對疫苗事件的關注,到今日,疫苗事件持續發酵。
此文對事件不作具體的評價,目的是梳理各方的進展和媒體的態度。
根據公開的報道,梳理疫苗事件如下:(2018年)7月5日,國家藥監局會同吉林省局對長春長生公司進行飛行檢查,在飛行檢查中發現,長春長生生物科技有限責任公司的凍干人用狂犬病疫苗生產存在記錄造假等嚴重違反《藥品生產質量管理規范》的行為。
7月15日,國家藥監局發布了《關于長春長生生物科技有限責任公司違法違規生產凍干人用狂犬病疫苗的通告》,同時,國家藥監局會同吉林省局組成調查組進駐企業全面開展調查。

經查明,長生生物存在編造生產記錄和產品檢驗記錄,隨意變更工藝參數和設備的現象。
國家藥監局已責令企業停止生產,收回藥品GMP證書,召回尚未使用的狂犬病疫苗。國家藥監局會同吉林省局已對企業立案調查,涉嫌犯罪的移送公安機關追究刑事責任。
而這是長春長生生物科技繼2017年10月被發現一批次百白破疫苗效價指標不符合標準規定之后,在不到一年的時間里再次出現嚴重違規行為。
根據《財經》的報道,7月20日,長生生物發布公告稱,其全資子公司長春長生生物科技有限責任公司收到《吉林省食品藥品監督管理局行政處罰決定書》,原因是該公司生產的“吸附無細胞百白破聯合疫苗”(批號:201605014-01),經食品藥品檢定研究院檢驗,檢驗結果“效價測定”項不符合規定。
吉林省食藥監局認為,長春長生行為違反《藥品管理法》第49條第一款“禁止生產、銷售劣藥”的規定,并已經于2017年10月27日立案調查。

而深圳證券交易所也已經向長生生物公司連續兩次下發關注函,要求長生生物公司說明長春長生公司生產疫苗情況。
7月20日,深交所啟動對長生生物公司及相關當事人公開譴責的紀律處分程序。深交所表示,經對公司(長生生物)信息披露情況進行全面梳理、核查,初步發現其未及時披露被有關機關調查的信息、內部控制存在重大缺陷。
7月22日,國家藥監局負責人通報長春長生違法違規生產凍干人用狂犬病疫苗案件有關情況。
7月22日晚間,長生生物回復深交所關注函稱,目前公司百白破生產車間已經停產,公司正積極研究百白破組份疫苗以及以此為基礎的多聯疫苗。將進行徹底整改,確保生產的合規性、真實性、可靠性、可追溯性以及疫苗質量的安全性。其還表示,“經自查,未曾收到吉林食藥監局出具的立案調查通知書”。

就在7月22日晚,因疫苗問題而備受關注的長生生物和康泰生物分別發布公告。長生生物表示,公司百白破生產車間已經停產。康泰生物則稱,與其他疫苗企業沒有股權關系和業務往來,公司與事件無關,經營有序,產品質量穩定,一切正常。
根據澎湃新聞的報道,在過去十多年中,不完全統計,長春長生及其母公司長春長生生物科技股份有限公司(002680,長生生物)至少涉入了12起受(行)賄案(注:受賄和行賄主體相同只計算一次),案情多為該公司銷售人員或者地方經銷商向當地負責疫苗采購的相關人員提供好處費、推廣費、回扣款,以獲得疫苗的優先采購或更大的采購份額。
而這12起案件集中發生在安徽、河南、福建、廣東四省,時間跨度從2001年至2017年。
截至7月22日,上海、河南、海南、重慶、山東、山西、廣西、河北這8個省市在內的疾控中心明確表示,全面停用、或是暫停使用長春長生狂犬病疫苗;湖南、福建、廣東這3省疾控中心表示,該省境內沒有涉事批次狂犬疫苗;西藏、北京、天津、江西四地疾控部門稱,未采購長春長生公司狂犬病疫苗產品或是采購此次涉事疫苗批次。
昨日(7月22日)晚間,李克強針對鬧得人心惶惶的疫苗事件再次作出批示:
此次疫苗事件突破人的道德底線,必須給全國人民一個明明白白的交代。
李克強在批示中要求,國務院要立刻派出調查組,對所有疫苗生產、銷售等全流程全鏈條進行徹查,盡快查清事實真相,不論涉及到哪些企業、哪些人都堅決嚴懲不貸、絕不姑息。對一切危害人民生命安全的違法犯罪行為堅決重拳打擊,對不法分子堅決依法嚴懲,對監管失職瀆職行為堅決嚴厲問責。盡早還人民群眾一個安全、放心、可信任的生活環境。
【上海鄰米網絡科技有限公司主營:商城開發,企業建站,APP開發,行業門戶網站(文庫系統,問答系統等)單商城多商城建站仿站等你來!我司有多套模板任你挑,價格從優,多買多得】